SNX-482
R 型(E-クラス)選択的 Ca2+チャネルブロッカー 新発売!
電位依存性 Ca2+ チャネルは、L、N、P/Q、R、および T 型に分類されています。これらのチャネルをコードする mRNA の解析により、それぞれのチャネルを構成する α1– サブユニットの構造も次々に明らかにされ、各チャネルを分子学的に取り扱うことが可能になってきています。最近では、体内にある天然型チャネルを用いた研 究はもとより、チャネルを人工的に発現し、各チャネルが関与する生体内機能を解明する仕事も蓄積されつつあります。これらの実験には選択的ブロッカーが必 須です。下の表に示したペプチド性ブロッカーはヘビ毒、イモ貝毒、あるいはクモ毒などから単離され、L、N、P/Q 型チャネルに選択性の高いこれらのブロッカーが広く使われてきました。また、R 型チャネル (α1-サブユニット α1E)に対するブロッカーとしては、ω-Agatoxin IIIA が知られていましたが、最近の研究で、このペプチドは、N、P/Q 型チャネルにも強い結合能を持ち、選択性の低いブロッカーであることが確認されています [J. Biol.Chem., 275, 21309 (2000)]。
1998年にアフリカ産タランチュラ (Hysterocrates gigas) から単離構造決定された“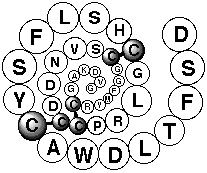 SNX-482”は 41 アミノ酸残基からなるペプチドで、分子内にある3組のジスルフィド結合は、1-4、2-5、および 3-6 のシステイン残基間に形成されていることが明らかにされています[Peptides 1998, 748 (1999)]。このペプチドは哺乳類細胞に発現したα1E-Ca2+ チャネルを15-30 nM (IC50) で阻害します。一方、下垂体後葉神経終末の R 型チャネル電流は抑制しますが、網膜神経節細胞、海馬錐体細胞などにおける電流には影響を与えないことも同時に解明され、R 型チャネルに対しては部位特異性があることも示唆されました[Biochemistry, 37, 15353 (1998)]。また、α1E-Ca2+ チャネルのバリアントに対しても同様な阻害活性の違いがあることも指摘されています[J. Neurosci., 20, 171 (2000)]。R 型チャネルに対する阻害作用の選択性は高く、L、N、P/Q、および T 型の Ca2+ チャネル、Na+ チャネル、および K+ チャネルは阻害しません[Biochemistry, 37, 15353 (1998)]。SNX-482 による神経伝達物質の放出への影響を調べた研究では、R 型チャネルはオキシトシンの放出のみに関わり、バソプレッシンの放出には関与しないことも明らかにされました[J. Neurosci., 19, 9235 (1999)]。
SNX-482”は 41 アミノ酸残基からなるペプチドで、分子内にある3組のジスルフィド結合は、1-4、2-5、および 3-6 のシステイン残基間に形成されていることが明らかにされています[Peptides 1998, 748 (1999)]。このペプチドは哺乳類細胞に発現したα1E-Ca2+ チャネルを15-30 nM (IC50) で阻害します。一方、下垂体後葉神経終末の R 型チャネル電流は抑制しますが、網膜神経節細胞、海馬錐体細胞などにおける電流には影響を与えないことも同時に解明され、R 型チャネルに対しては部位特異性があることも示唆されました[Biochemistry, 37, 15353 (1998)]。また、α1E-Ca2+ チャネルのバリアントに対しても同様な阻害活性の違いがあることも指摘されています[J. Neurosci., 20, 171 (2000)]。R 型チャネルに対する阻害作用の選択性は高く、L、N、P/Q、および T 型の Ca2+ チャネル、Na+ チャネル、および K+ チャネルは阻害しません[Biochemistry, 37, 15353 (1998)]。SNX-482 による神経伝達物質の放出への影響を調べた研究では、R 型チャネルはオキシトシンの放出のみに関わり、バソプレッシンの放出には関与しないことも明らかにされました[J. Neurosci., 19, 9235 (1999)]。
今後、この SNX-482 を用い、Ca2+ チャネルの関与した生体内機能が、より詳細に解明されるものと期待されています。
| コード | 製品名 | 包装・容量 |
| 4363-s | SNX-482 | 0.1 mg vial |
L、N、P、および Q 型チャネルに対するペプチド性ブロッカー
| コード | ブロッカー | 選択性 | 包装・容量 |
| 4255-s | Calciseptin | L-type | 0.1 mg vial |
| 4310-s | Calcicludine | L-type | 0.1 mg vial |
| 4161-v | ω-Conotoxin GVIA | N-Type | 0.5 mg vial |
| 4289-v | ω-Conotoxin MVIIA | N-Type | 0.5 mg vial |
| 4284-v | ω-Conotoxin SVIB | N-Type | 0.5 mg vial |
| 4256-s | ω-Agatoxin IVA | P-Type | 0.1 mg vial |
| 4294-s | ω-Agatoxin TK | P-Type | 0.1 mg vial |
| 4283-v | ω-Conotoxin MVIIC | P/Q-Type | 0.5 mg vial |

